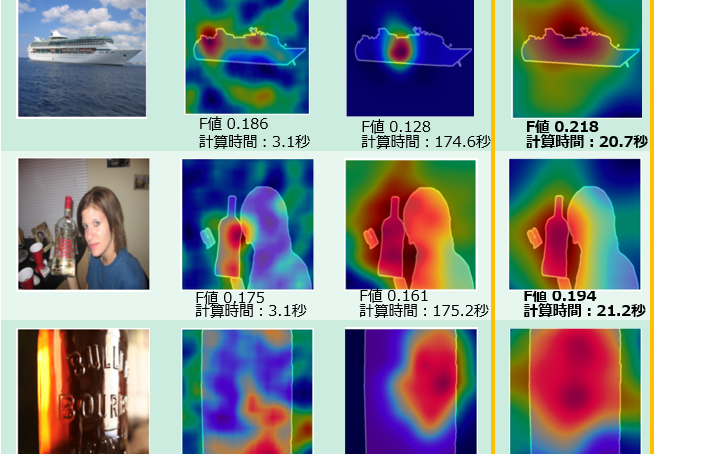
【最新発明情報】固形腫瘍内部の低酸素状態をモニタリングできる血中バイオマーカー(および創薬標的)
病態やその治療有効性等を把握・予測するにあたり、腫瘍組織内の低酸素領域の量や低酸素の程度を測定することができる新規バイオマーカー及びその測定方法を提供します。また、がん細胞の放射線治療抵抗性を抑制するための新規治療標的を提供します。
背景
固形腫瘍内部には低酸素状態となっている領域(酸素分圧が低下した領域)が存在し、低酸素状態は放射線治療や抗がん剤治療に対するがん細胞の抵抗性を誘導する重要な環境要因であることが知られています。また、酸素濃度が低いほど病態が悪化した状態にあるともいわれています。病態やその治療有効性等を把握、予測するにあたり、また、がん患者毎に最適な治療を提供する個別化医療を実現するにあたり、腫瘍内の低酸素領域の量や低酸素の程度等を知ることは重要であるといえます。
発明概要と利点
発明者らは、低酸素刺激依存的に”ある分子A”の発現・分泌量が増加することを見出しました(図1)。また、分子Aの血中濃度が腫瘍内低酸素領域の量に相関することを確認しました(図2)。さらにこの分子Aが、がん細胞の放射線抵抗性を高める機能も持っていることを確認しました(図3)。これらの結果から、この分子Aが”腫瘍内低酸素”や”腫瘍の増悪性”を予測する『侵襲性の低い血中バイオマーカー』として、また放射線治療の効果を高めるための『治療標的』として有用なことが確認されました。
A
B
C
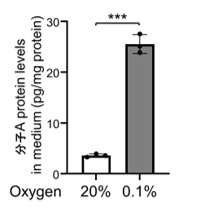
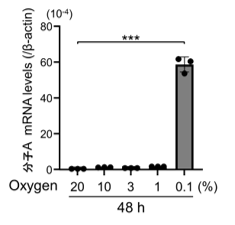
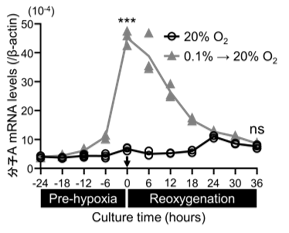
図1.低酸素刺激を受けたがん細胞は、分子Aを発現・分泌する
ヒト子宮頸がん由来HeLa細胞は、低酸素刺激に鋭敏に応答して分子Aの発現を誘導し(A, B)、細胞外に分子Aを分泌した(C)。
A
B

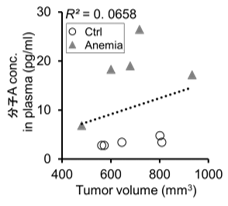
図2.“悪性固形腫瘍内の低酸素領域の量”と“血中の分子Aの濃度”は相関する
HeLa細胞を移植して準備した担がんマウスに溶血剤(フェニルヒドラジン)を投与して、低酸素領域の量が異なる移植腫瘍を人為的に準備した。血中の分子Aの濃度は腫瘍体積には相関せず(A: R2 = 0.0658)、腫瘍内の低酸素領域の量(内在性の低酸素マーカーCA9の発現量)と相関した(B: R2 = 0.7744)。
A
B
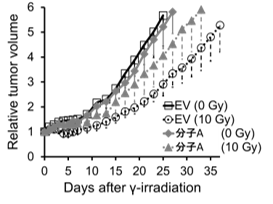
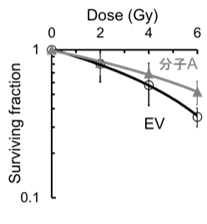
図3.分子Aはがんの放射線抵抗性を亢進する
コロニー形成試験により、分子Aの過剰発現ベクター(分子A)を導入したHeLa細胞が、空ベクター(EV)を導入した細胞と比較して、放射線抵抗性を獲得することが確認された(A)。これらの細胞を移植した担癌マウスに対してガンマ線の局所治療を実施し、その後の腫瘍増殖を測定した。分子Aの過剰発現により放射線治療後の腫瘍再増殖が早まることが確認された(B)。
研究段階
in vitro/in vivoでの各種評価
- 低酸素刺激を受けたがん細胞が分子Aを発現し、血中に分泌すること
- 血漿中に分泌された分子Aの濃度を指標に、腫瘍内の低酸素分画をモニターできること
- 分子Aががんの放射線治療抵抗性を高めること
適応分野
- 体外診断薬
- 試薬
- 創薬・製薬(創薬標的)
希望の連携形態
- 実施許諾契約
- オプション契約(技術検討のためのF/S)
※本発明は京都大学から特許出願中です。
ライセンス契約を受けていただき 本発明の実用化を目指していただける企業様を募集しています。ぜひ、お問い合わせください。
固形がんの内部の低酸素状態をモニタリングできるバイオマーカーを提供します。また放射線治療抵抗性にも関係します。
京都大学産学連携担当(株式会社TLO京都)担当:鈴木 祥宏より